
医学研究中,精准预测手术效果一直是临床决策的核心挑战。成人脊柱畸形(ASD)手术虽能改善患者生活质量,但术后并发症频发、恢复效果参差不齐的问题长期困扰着医生和患者。近期发表于Bone & Joint Journal (中科院1区,IF=4.9)的一项研究,通过机器学习技术成功开发了一款预测模型,为这一难题提供了创新解决方案。本文将从研究背景的创新点、实验设计的巧妙思路,以及未来临床应用的潜力三个方面,为希望借鉴顶刊经验的医生解析这一研究的核心价值。首都医科大学宣武医院骨科主任鲁世保教授团队完成了此项成果。

传统预测的局限与机器学习的突破
ASD手术的目标是矫正脊柱形态、缓解疼痛并提升患者生活质量,但现实情况是,仅约半数患者能达到“理想手术效果”(ISO),即术后生活质量显著提升且无并发症。传统统计方法虽能识别部分风险因素(如年龄、骨密度),但其预测能力有限,且多数因素(如遗传、解剖结构)难以干预,临床实用性大打折扣。
这项研究的创新之处在于,首次将机器学习引入ASD手术预后预测。与传统方法不同,机器学习能捕捉复杂非线性关系,并通过特征重要性分析筛选出可干预的临床指标。例如,团队发现抑郁、骨质疏松、术后骶骨倾斜匹配等八个关键因素中,多数可通过术前干预(如抗抑郁治疗、抗骨质疏松药物)或手术规划(如个性化脊柱对位目标)进行优化。这一发现将预测模型从“理论工具”转化为“临床行动指南”,极大提升了实用性。
实验设计:数据驱动的模型构建与验证
研究的巧妙设计体现在三个层面:数据筛选、特征选择与模型优化。
首先,团队严格筛选了458例ASD手术患者,最终纳入208例符合长期随访条件的病例。通过排除合并症(如帕金森病、强直性脊柱炎)和短期随访数据,最大限度减少混杂因素干扰。这种“以质量换数量”的策略,确保了数据的可靠性和结论的稳健性。
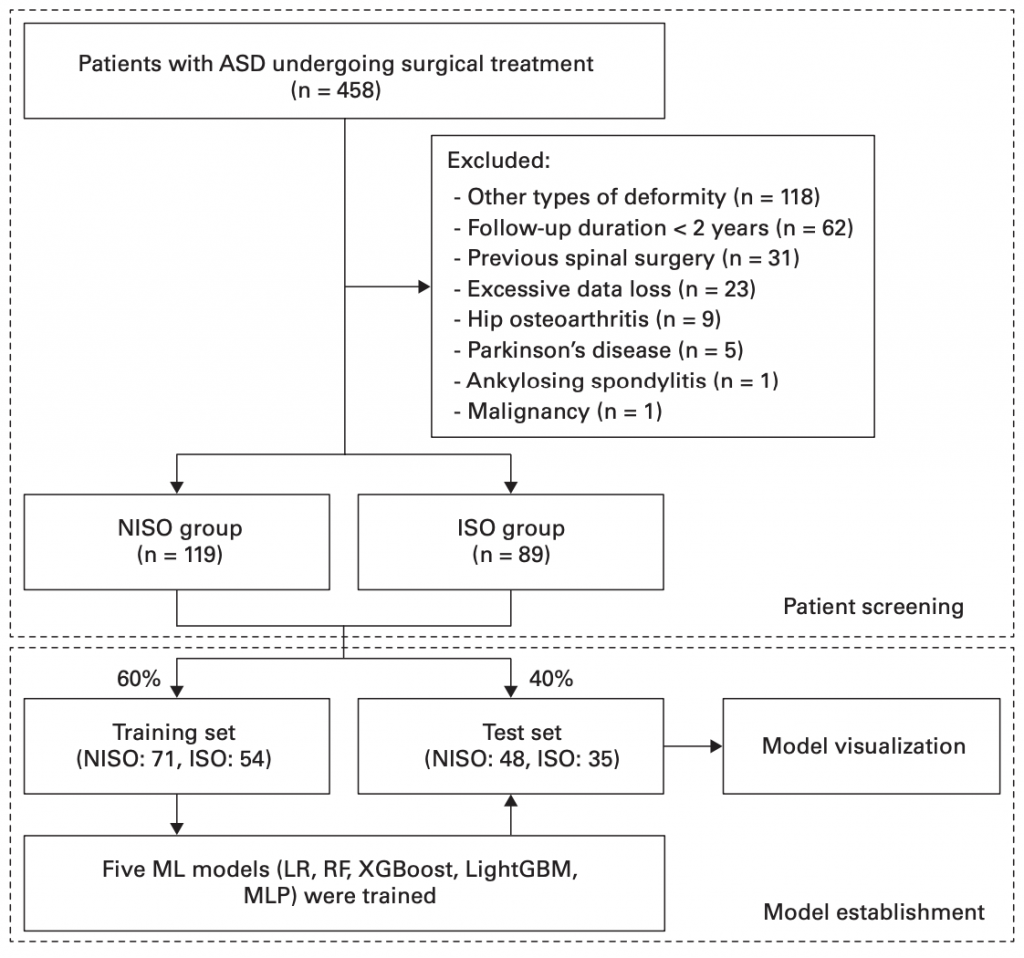
图:人群选择与模型开发
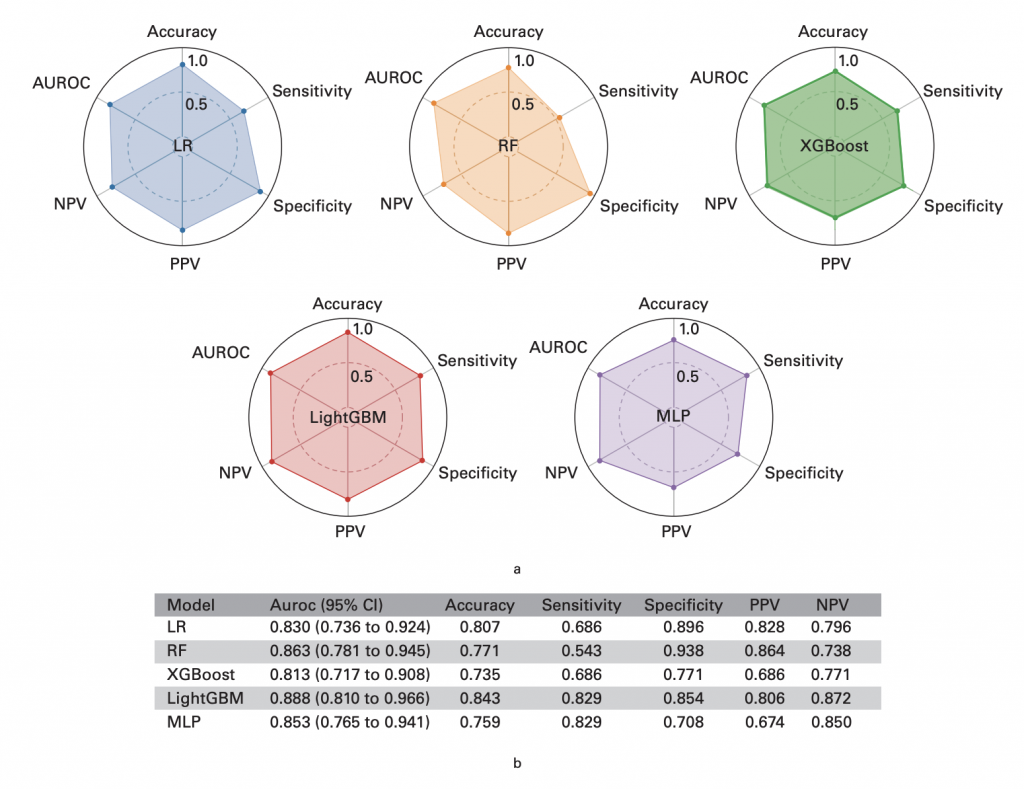
图:机器学习模型的性能指标
其次,研究采用三种特征选择方法(LASSO、RFE、Boruta)交叉验证,从43个候选变量中锁定8个关键预测因子。这种多算法交叉验证的方法,既避免了单一方法的偏差,又突出了最具临床意义的指标。例如,“骨盆代偿失败”这一指标此前常被忽视,但机器学习模型揭示其与术后并发症的强相关性,提示医生需在术前评估骨盆代偿能力。
最后,团队对比了五种机器学习模型(逻辑回归、随机森林、XGBoost等),最终选择LightGBM作为最优模型。其AUROC值高达0.888,敏感性和特异性均超过80%,显著优于传统方法。这一过程展示了如何通过算法竞争与超参数调优(如网格搜索、交叉验证)提升模型性能,为医生设计类似研究提供了方法论范本。
从预测模型到临床实践
研究的结论不仅验证了模型的准确性,更揭示了临床优化的新方向。例如,针对筛选出的可干预因素,团队提出以下策略:
- 术前多学科评估:通过双能X线骨密度检测、抑郁量表(如Zung量表)筛查患者身心状态,针对性使用特立帕肽改善骨密度,或通过认知行为疗法缓解抑郁。
- 个性化手术规划:基于“矢状面年龄校正评分(SAAS)”设定脊柱对位目标,避免过度矫正或矫正不足,从而降低近端交界性后凸(PJK)等机械并发症风险。
- 跨模态数据整合:未来可纳入影像组学、基因组学数据,进一步提升模型预测能力。
此外,研究团队指出了当前局限性:单中心回顾性设计可能限制模型泛化性,需通过多中心前瞻性研究验证。这一思路提示医生,若希望复现类似研究,需在数据多样性(如不同人种、医疗条件)和长期随访设计上投入更多资源。
总之,这项研究不仅为ASD手术提供了实用工具,更展示了机器学习在临床研究中的潜力。对于希望发表高水平论文的医生而言,关键在于从临床问题出发,以数据驱动的方法突破传统局限,并通过严谨设计将结果转化为可操作的临床指南。未来,随着人工智能与精准医学的深度融合,类似的预测模型或将成为外科决策的“标准配置”,而掌握这一技术的医生,无疑将在科研与临床的双重赛道中占据先机。
